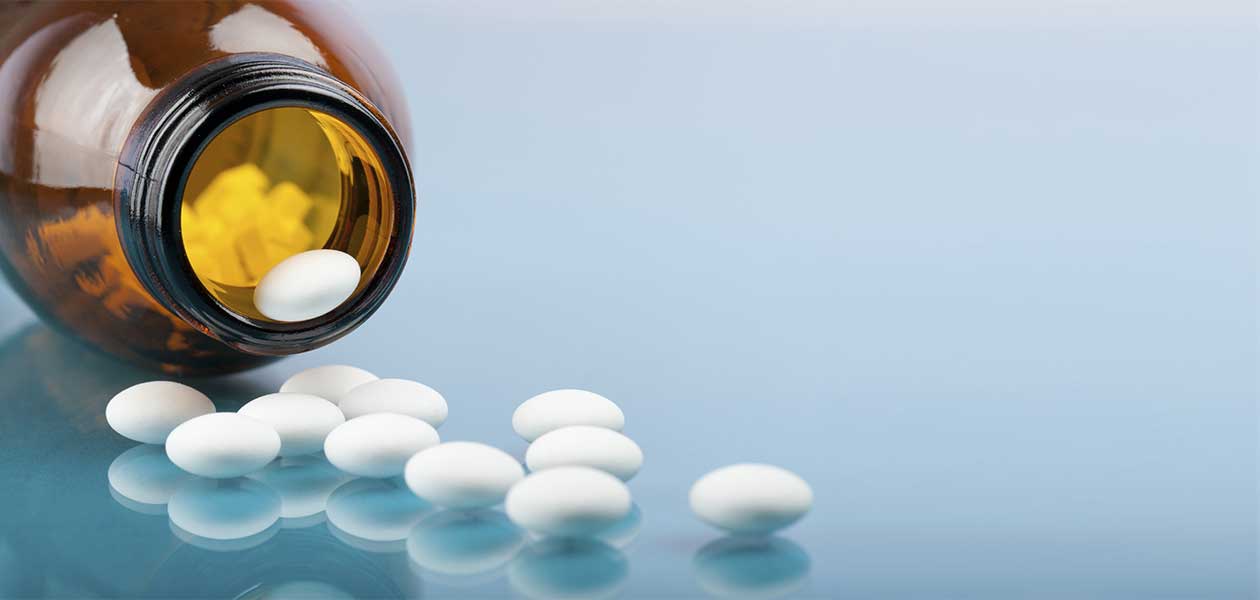
L’EMA, Agenzia Europea del Farmaco, ha approvato la commercializzazione della mexiletina con il nome di NaMuscla per i pazienti affetti da miotonia non distrofica (miotonia congenita di Thomsen o di Becker da canalopatia del cloro; paramiotonia congenita; miotonia aggravata dal potassio da canalopatia del sodio). La tappa successiva sarà l’autorizzazione del nuovo farmaco da parte dell’AIFA, Agenzia Italiana del Farmaco. Per il momento lo stesso farmaco non è stato approvato per le distrofie miotoniche nella quali la compromissione cardiaca ne impedisce l’erogazione su ampia scala perchè comporta un attento monitoraggio del cuore da parte dei centri prescrittori. Hanno contribuito al risultato la casa farmaceutica svizzera Lupin e anche il prof. Meola, che ha partecipato alla stesura della documentazione per l’approvazione finale, presentata all’EMA a Londra nel luglio 2018.

Distrofia Miotonica: consigli alimentari e per la deglutizione
La difficoltà nella deglutizione è uno dei problemi causati dalla miotonia nelle distrofie miotoniche. Alcuni consigli utili per gestirla